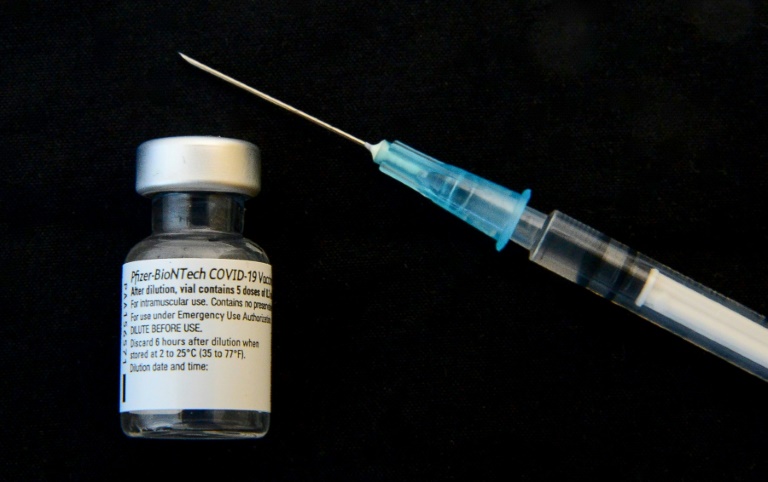
Der Corona-Impfstoff von Biontech ist nach Angaben des Mainzer Unternehmens gegen die wichtigsten Virus-Mutanten aus Großbritannien und Südafrika wirksam. Erste Ergebnisse von In-Vitro-Tests wiesen darauf hin, dass die Entwicklung eines neuen Impfstoffs für diese Varianten nicht notwendig sei, teilten Biontech und sein US-Partner Pfizer am Donnerstag mit. Derweil ging der Streit um die Lieferungen des Impfstoffs von Astrazeneca, über dessen EU-weite Zulassung am Freitag entschieden werden soll, weiter.
Biontech und Pfizer untersuchten nach eigenen Angaben verschiedene Coronavirus-Varianten auf Grundlage der erstmals in Großbritannien und Südafrika aufgetretenen Mutationen. Dabei sei die Neutralisierung bei drei Mutanten der südafrikanischen Variante „geringfügig niedriger“ ausgefallen. Es sei jedoch unwahrscheinlich, dass dies „zu einer signifikanten Verringerung der Wirksamkeit“ des Impfstoffs führe, betonten die Unternehmen.
Biontech und Pfizer erklärten, dass es sich zunächst um erste Tests zu den neuen Mutationen handelte. Diese sollten fortgesetzt werden; die bisher festgestellten und auch mögliche neue Virus-Varianten würden weiterhin auf mögliche Resistenzen gegen den Impfstoff beobachtet. Sollte es notwendig sein, könnte der Impfstoff angepasst werden.
Die neuen Varianten des Coronavirus breiten sich in immer mehr Ländern aus. Nach Angaben der Weltgesundheitsorganisation (WHO) wurde die zunächst in Großbritannien registrierte Mutante inzwischen in mindestens 70 Ländern nachgewiesen. Sie ist Wissenschaftlern zufolge ansteckender als die Ursprungsvariante des Coronavirus. Auch für die zunächst in Südafrika nachgewiesene Mutante verzeichnete die WHO ein größeres Verbreitungsgebiet.
Am Montag hatte bereits der US-Hersteller Moderna erklärt, dass sein Impfstoff gegen die britische und die südafrikanische Variante wirkt. Die Produkte von Biontech/Pfizer und Moderna sind derzeit die einzigen beiden EU-weit zugelassenen Vakzine gegen das Coronavirus. Am Freitag will die europäische Arzneimittelbehörde EMA über die Zulassung des Impfstoffs des britisch-schwedischen Pharmakonzerns Astrazeneca entscheiden, der in Zusammenarbeit mit der Universität Oxford entwickelt wurde.
Bereits vor der EMA-Entscheidung empfahl die Ständige Impfkommission des Robert-Koch-Instituts, dass das Astrazeneca-Produkt im Gegensatz zu den beiden bereits zugelassenen Vakzinen nur an Menschen unter 65 Jahren verabreicht werden soll. Sie begründete ihre Einschätzung damit, dass zur Beurteilung der Impfeffektivität ab 65 Jahren „aktuell keine ausreichenden Daten“ vorlägen. „Abgesehen von dieser Einschränkung wird dieser Impfstoff ebenfalls als gleichermaßen geeignet angesehen“, hieß es in der Empfehlung.
Zugleich tobte ein heftiger Streit über die Liefermengen für die Europäische Union (EU): Astrazeneca hatte in der vergangenen Woche mitgeteilt, wegen Produktionsproblemen in einem Werk in Belgien vorerst deutlich weniger Impfstoff liefern zu können als vorgesehen. Nach Angaben aus EU-Kreisen würden deshalb im ersten Quartal 75 Prozent weniger Dosen geliefert als vereinbart. Brüssel kritisiert, dass die Lieferungen an Länder außerhalb der EU wie Großbritannien nicht eingeschränkt werden.
Am Donnerstag sagte ein Sprecher der EU-Kommission in Brüssel, Astrazeneca habe noch immer keine Lösung präsentiert, wie die Lieferengpässe bei seinem Corona-Impfstoff beseitigt werden könnten. Es sei an dem Unternehmen, Vorschläge zu machen, wie es die Verpflichtungen aus seinem Liefervertrag erfüllen wolle.
Bundesgesundheitsminister Jens Spahn (CDU) verwies im NDR darauf, dass die EU Astrazeneca mit über 300 Millionen Euro beim Aufbau der Produktion unterstützt habe. „Es kann immer was passieren, die Produktion von Impfstoffen ist sehr komplex“, sagte er. „Aber dann muss es alle, die bestellt haben, gleich betreffen und nicht nur die Europäische Union.“
Quelle: AFP